ここからヘッダーメニューです。



ここからサイト内検索です。
ここから共通メニューです。 ここまで共通メニューです。





嗜銀顆粒病(Argyrophilic Grain Disease)は、脳神経細胞に「嗜銀顆粒」と呼ばれる物質が蓄積することで起こる病気を指します。この病気により認知症の症状が現れたものを嗜銀顆粒性認知症(Argyrophilic Grain Dementia:AGD)と呼びます。
高齢者の約5-9%、100歳以上の実に31.3%が嗜銀顆粒病との報告があります。
また、認知症患者の約5%程度が嗜銀顆粒性認知症との報告もあり、アルツハイマー型認知症やLewy小体型認知症に次ぐ頻度となっています。
嗜銀顆粒性認知症(AGD)は、他の認知症に比べ①高齢発症・緩徐な進行、②軽度記憶障害、③性格の変化を特徴とします。
嗜銀顆粒性認知症(AGD)の病態機序(病気が出来上がっていく仕組み)は、異常タウ蛋白の一種である嗜銀顆粒が脳に沈着し、認知機能低下や性格変化を来たすことを特徴とする神経変性疾患です。
タウ蛋白は通常、微小管に結合することで神経細胞の構造維持や機能を安定化させる役割を担っています。このタウ蛋白が異常にリン酸化されると、正常な機能を失い凝集し、神経細胞内に沈着するようになります。この蓄積により神経細胞が機能不全を起こし、さまざまな神経変性疾患の発症の原因となるとされています。
異常タウ蛋白には3リピートタウ(3Rタウ)と4リピートタウ(4Rタウ)の2種類があり、どちらが優位に蓄積するかで発症する病気が異なります。3Rタウの蓄積は進行性核上性麻痺(PSP)、球状グリア性タウオパチー(GGT)に関与し、4Rタウの蓄積は嗜銀顆粒性任認知症(AGD)、大脳皮質基底核変性症(CBD)に関与します。これらの疾患はそれぞれがオーバーラップすることもあります。嗜銀顆粒性認知症は、特に大脳皮質基底核変性症に高頻度に合併するとされています。
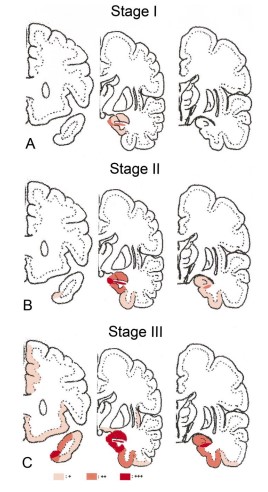 図1 Saitoらによる嗜銀顆粒のステージ分類より引用
図1 Saitoらによる嗜銀顆粒のステージ分類より引用
嗜銀顆粒はまず初めに迂回回(側頭葉内側面の前方に位置)に出現し、その後側頭葉を中心として緩徐進行性に拡大していきます。この広がりはSaitoらによって以下のようにステージ分類されています。
臨床的意義として、StageⅢの範囲で嗜銀顆粒が存在数する場合、71.2%の症例でCDR(Climocal Dementia Rating)1以上の認知症を呈し、97%の症例でCDR0.5以上の認知機能障害を認めるとされています。
嗜銀顆粒性認知症(AGD)の確定診断は、死後脳の病理学的検査で行われますが、臨床的には画像検査やバイオマーカーの分析等を用いて総合的に診断しています。
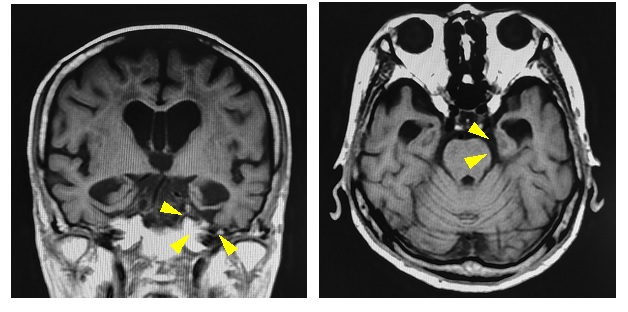
図2 嗜銀顆粒性認知症患者のMRI冠状断・軸位断画像 左優位に迂回回の萎縮を認める※当院例
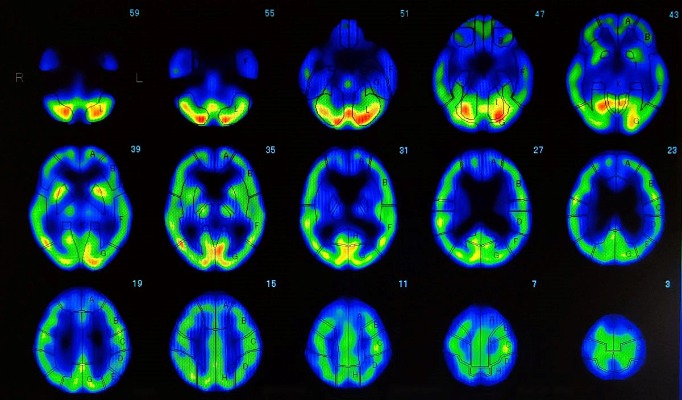
図3 AGD患者のSPECTによる脳血流の定性評価 側頭葉内側部を中心とした血流低下を認める※当院例
AGDでは脳脊髄液中のアミロイドβは正常範囲内であり、総タウ及びリン酸化タウの上昇もごく軽度にとどまるとされています。
一方のアルツハイマー型認知症では、発症約25年前から脳にアミロイドβが沈着するため、脳脊髄液中のアミロイドβは低下し、発症約15年前から総タウおよびリン酸化タウは上昇します。
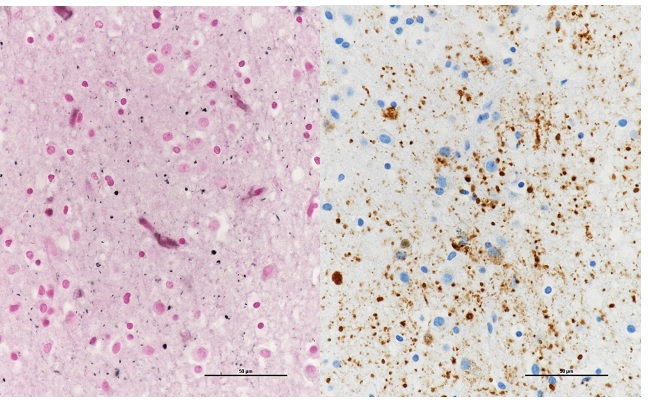
図4(左):Gallyas-Braak染色、図5(右):リン酸化タウ免疫染色
東京都健康長寿医療センター 老年病理学研究チーム 齊藤祐子医師より提供
嗜銀顆粒性認知症(AGD)に特異的な治療法は現在のところ存在しません。治療は、アルツハイマー型認知症に準じて行われることが多いものの、AGDではコリンエステラーゼ阻害薬の効果がアルツハイマー型認知症やLewy小体型認知症ほどは期待できないのが現状です。また易怒性などが顕在化する場合もみられます。しかし、AGDが疑われる場合でも、他の認知症、特にアルツハイマー型認知症の合併の可能性を考慮し、それに対する治療を行うことが重要です。
前述のようにAGDでは、頑固さや易怒性などの性格の変化が出現することがあります。患者さんは特定の人を好む、または嫌う傾向が強くなり、自分に共感してくれる人や安心感を与えてくれる人を特に好むようになることがあります。このような変化は、病気の一部であることを理解することが大切です。
幸いなことに、AGDは他の認知症に比べて進行が遅いという特徴があります。適切なケアと周囲の理解があれば、患者さんが長期にわたって家庭で過ごすことができる可能性が高くなります。患者さんの個性や尊厳を尊重しながら、家族や周囲の人々が協力して支えていくことが必要です。
当院では、AGDの診断や薬物療法に加え、必要に応じて入院によるリハビリテーションや環境調整を行い、患者さんの生活の質を向上させるための包括的な治療を提供しています。